Антифосфолипидный синдром
Содержание:
Основные сведения
Фосфолипиды – базовая составляющая мембран всех живых клеток организма и тромбоцитов. По своей структуре это сложные жиры, состоящие из фосфорной кислоты, жирных кислот и азота. По функции – источник фосфорной кислоты, необходимой для нормальной жизнедеятельности организма. Кроме того, фосфолипиды обеспечивают пластичность клеточной мембраны, в то время как холестерин делает ее жесткой. Поэтому соединение «фосфолипиды-холестерин» определяет либо упругость, либо тягучесть мембран клеток. Также фосфолипиды принимают активное участие в поддержании жиров в растворимом состоянии, т.е. они являются своеобразными «растворителями» для высокогидрофобных соединений, в т.ч. и для холестерина. Это же свойство позволяет им поддерживать степень литогенности желчи (склонность желчи к образованию желчных камней) и снижать риск образования холестериновых желчных камней. Но главной задачей фосфолипидов является регуляция процессов свертывания крови, хотя механизм их действия для специалистов пока остается не до конца ясным.
В некоторых случаях фосфолипиды становятся объектом агрессии собственного организма, когда иммунитет не распознает их как «своих» и начинает вырабатывать антитела, призванные уничтожить «чужеродные» клетки. Аутоиммунная реакция сопровождается симптомокомплексом, который в медицинских кругах называется синдромом Хьюза-Стовина или антифосфолипидным синдромом (АФС). На практике данное состояние проявляется рядом патологий беременности, особенно, в третьем триместре, у женщин и развитием тромбоза вен и инфаркта миокарда – у молодых мужчин.
АФС может быть вторичным при некоторых аутоиммунных заболеваниях, например, быть следствием системной красной волчанки (СКВ), или первичным, т. е. развиваться самостоятельно, без каких-либо сопутствующих патологий. Нередко антитела к фосфолипидам обнаруживаются при ВИЧ-инфекции, отдельных онкологических заболеваниях, а также появляются на фоне приема лекарственных препаратов: новокаинамид, фенотиазины и пр.
Таким образом, диагностика АФ-синдрома должна проводиться комплексно, т. е. включать в себя дополнительные клинические параметры. Анализ крови на АФС – это иммуноферментное исследование, которое позволяет своевременно диагностировать аутоиммунные нарушения, назначать правильное лечение и контролировать его эффективность, а также профилактировать возможные осложнения болезни.
АФС при СКВ в детском возрасте
Частота АФС при СКВ у детей составляет 35%, что совпадает с его распространенностью у взрослых с этой патологией . Частота развития тромбозов у больных СКВ зависит от типа обнаруживаемых у них аФЛ-АТ: при наличии ВА она равна 61%, в случае обнаружения аКЛ – 52%, при их отсутствии – 24%.
Анализ течения АФС у детей с СКВ показал, что симптомы синдрома Hughes могут появиться в любом периоде заболевания, причем у 20% лиц его признаки наблюдаются уже в дебюте CКВ.
Спектр клинических и лабораторных признаков АФС при СКВ у детей представлен в таблице 2. У детей с СКВ и АФС по частоте преобладает тромбоз мелких сосудов кожи. Кожные симптомы могут быть первым его проявлением у пациентов, у которых в дальнейшем развивается мультисистемный тромбоз.
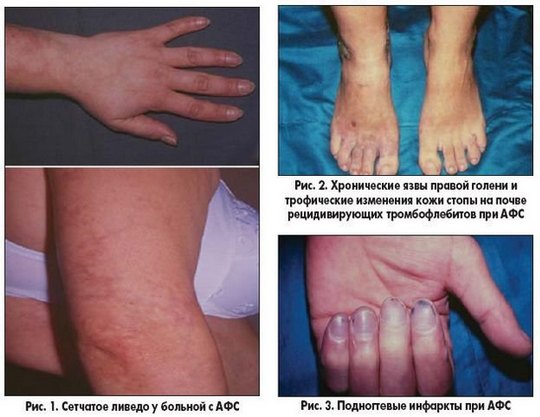
Характерный признак АФС у детей – сетчатое ливедо, часто в сочетании с церебральной патологией (синдром Снеддона). Вместе с тем ливедо отмечается и при других аутоиммунных процессах (узелковом полиартериите, криоглобулинемии), инфекциях, а также в мягкой форме у девочек-подростков, что требует дифференциации .
Яркое проявление АФС у детей – дистальная ишемия кожи, проявляющаяся стойкими эритематозными или лиловыми пятнами на пальцах рук и ног и в некоторых случаях сопровождающаяся дигитальным некрозом. У детей реже, чем у взрослых, наблюдаются такие проявления АФС, как тромбоз вен конечностей и хронические язвы голеней и стоп.
Среди неврологических нарушений наиболее часто при СКВ у детей отмечаются признаки ишемической энцефалопатии, нарушение когнитивных функций, психические расстройства, мигренеподобные цефалгии, реже – эписиндром, хореические гиперкинезы, транзиторные нарушения мозгового кровообращения (табл. 2).
У детей с СКВ и аФЛ-АТ отмечается повышенная частота вегетаций на клапанах и митральной регургитации, которые могут быть источником эмболизации. Часто выявляются признаки нарушения коронарного кровообращения и легочной гипертензии. Развитие последней при наличии аФЛ-АТ может быть связано с тромбозом сосудов легких in situ.
Ведение беременности при АФС
Чтобы во время беременности не возникало тромбозов и потери плода, необходима профилактика – немедикаментозная и медикаментозная.
Немедикаментозная:
физическая активность стимулирует собственный тканевой плазминоген;
эластичный медицинский трикотаж 1-2 класс компрессии;
диета с большим количеством растительных масел, свеклы, чернослива, инжира, бананов, поскольку эти продукты обладают слабительным эффектом – это важно, чтобы при дефекации не создавать повышенное давление на стенки вен.
Медикаментозная профилактика тромбозов при беременности
Существует несколько вариантов профилактики в зависимости от течения антифосфолипидного синдрома.
- Отсутствуют серологические маркеры ВА и антикардиолипиновый антиген, тромботические осложнения, могут определяться антитела к бета2-гликопротеину I.
- В первом триместре назначают Клексан или Фрагмин в дозировке для оптимального поддержания д-димеров и фолиевая кислота 4 мг/кг.
- Второй и третий триместры – Фригмин или Клексан до нормальных цифр д-димеров, рыбий жир, Аспирин 75-100 мг/кг при повышенной агрегации тромбоцитов, СЗП 10 мл/кг или концентрат антитромбина при снижени антитромбина 3 менее 80%.
- Перед родами Аспирин отменяют за 3-5 суток, вечернюю дозу НМГ меняют на СЗП 10мг/кг с гепарином 1-2 Ед на каждый мл СЗП.
- При родоразрешении – нормальный уровень д-димеров СЗП 10 мг/кг, при высоком уровне перед операцией – СЗП 5 мл/кг плюс гепарин 1 Ед на 1 мл СЗП или концентрат антитромбина 3, во время операции СЗП 5 мл/кг.
- При наличии в крови АФЛА и тромбозами или без них, отсутствует волчаночный антикоагулянт.
- 1 триместр – Клесан или Фрагмин для поддержания нормального уровня д-димеров+фолиевая кислота 4 мг/сутки.
- 2 и 3 триместры – Клексан или Фрагмин в индивидуальных дозировках+Аспирин 75 мг/сутки+рыбий жир 1-2 кап 3 раза в день, при снижении антитромбина 3 менее 80% активности – СЗП 10 мл/кг или концентрат антитромбина Ⅲ – 10-50 МЕ/кг, при повышении д-димеров более 0,5 мкг/мл – повышении дозировки НМГ.
- Перед родами – отмена Аспирина за 3-5 дней, НМГ заменяют на СЗП 10 мл/кг+НФГ 1-2 ЕД на каждый мл СЗП, при повышении антифосфолипидных антител назначается Преднизолон (Метилпред) 1-1,5 мг/кг внутривенно.
- При родоразрешении если нормальные D-димеры – СЗП 10 мл/кг; если повышены д-димеры, то до операции СЗП 5 мл/кг+НФГ 1 ед на каждый мл CPG или концентрат антитромбина 3, во время операции – СЗП 5 мл/кг, при значительном повышении антител – Преднизолон 1,5-2 мл/кг внутривенно.
- При повышении ВА от 1,5 до 2 усл.ед.
- 1 триместр – базовый прием Фрагмин или Клексана в дозе, как в прошлом варианте+фолиевая кислота+иммуноглобулин человеческий 25 мл через день 3 дозы в 7-12 нед. Если имеется повышение ВА более 1,5 усл.ед в первом триместре, то беременность стоить прервать.
- 2 и 3 триместр – Фрагмин и Клексан в дозировке для нормального поддержания д-димеров+Аспирин 75 мг+рыбий жир 1-2 кап 3 раза в день, при сниженном антитромбине – СЗП 10 мл/кг или концентрат антитромбина Ⅲ 10-50 МЕ/кг в/в, при повышении Д-димеров – повысить дозировку НМГ, иммуноглобулин 25 мл через 1 день 3 раза в 24 недели, если повышен ВА от 1,2 до 2 усл.ед – Преднизолон 30-60 мг/сут в/в, с 13 до 34 недели возможен перевод на Варфарин под контролем МНО.
- Перед родами если был Варфарин, то его отменяют за 2-3 нед, переводят на НМГ, Аспирин отменяется за 3-5 дней до родов, СЗП 10 мл/кг+НФГ 2 ед на каждый мл плазмы, Преднизолон – 1,5-2 мл/кг в/в, при сниженном антитромбине Ⅲ – концентрат антитромбина Ⅲ 10-30 МЕ/кг.
- При родах – до операции СЗП 500 мл+НФГ 1000 ЕД, во время операции – СЗП 10 мл/кг, Преднизолон 1,5-2 мг/кг в/в.
- При повышении ВА более 2 усл.ед беременность следует прерывать.
Если у женщины развился катастрофический антифосфолипидный или HELLP-синдром, то может быть назначен плазмоферез или плазмофильтрация.
ЛЕЧЕНИЕ
• Профилактика и лечение АФС — сложная задача (табл. 46-2). Это связано с неоднородностью патогенетических механизмов, лежащих в основе АФС, полиморфизмом клинических проявлений, отсутствием достоверных клинических и лабораторных показателей, позволяющих прогнозировать рецидивирование тромботических нарушений. Риск рецидивирования тромбозов особенно высок у больных молодого возраста с персистирующими высокими уровнями АТ к кардиолипину, волчаночного антикоагулянта и при одновременном обнаружении АТ к кардиолипину и волчаночного антикоагулянта, а также при наличии рецидивирующих тромбозов и/или акушерской патологии в анамнезе, при наличии других факторов риска тромботических нарушений (АГ, гиперлипидемия, курение, приём оральных контрацептивов), при высокой активности СКВ, при быстрой отмене непрямых антикоагулянтов, при сочетание высоких титров АТ к фосфолипидам с другими нарушениями свертывания.
• Общие рекомендации по ведению больных с АФС представлены в табл. 46-2.
Таблица 46-2 Общие рекомендации по профилактике и лечению тромбозов у пациентов с АФС
Симптоматика
Антифосфолипидные синдромы состоят из большого количества самых разнообразных клинических проявлений, которые будут отличаться в зависимости от поражённого сегмента.
Самым первым и распространённым признаком болезни выступает формирование тромбов, которые могут быть венозными (встречаются в несколько раз чаще) и артериальными. Наиболее часто в патологию вовлекаются вены ног, печени, почек и сетчатки, а также церебральные артерии.
Тромбоз вен нижних конечностей имеет такие признаки:
- интенсивный болевой синдром;
- отёчность;
- покраснение кожных покровов поражённого сегмента;
- образование гангрен и язв на больной ноге.
Тромбы ног могут отсоединяться от стенок сосудов и с потоком крови достигать лёгочной артерии, что приводит к появлению:
- лёгочного кровотечения;
- лёгочной гипертензии;
- тромбоэмболии.
При поражении почек и печени симптомы будут следующими:
- увеличение объёмов того или иного органа;
- скопление большого количества жидкости в брюшине, что также носит название асцит;
- изменение состава крови, а именно понижение концентрации калия и холестерина;
- признаки портальной гипертензии.
Если патология затрагивает ЦНС, то симптоматическая картина будет включать в себя:
- мигрень;
- гиперкинезы;
- судороги;
- тугоухость;
- нейропатию зрительного нерва;
- повышение АД.
Помимо этого, в симптоматику АФС входят:
- кровоизлияния в ЖКТ;
- инфаркт селезёнки;
- кожная эритема с локализацией на ладонях и стопах;
- сетчатое ливедо;
- гангрена пальцев;
- появление трофических язв на кожном покрове;
- двигательная слабость;
- потеря зрения;
- общая амнезия;
- малокровие;
- нарушение ЧСС.
Весь вышеуказанный симптомокомплекс характерен как для взрослых, так и для детей, однако у последней категории пациентов патология протекает тяжелее.
Антифосфолипидный синдром у беременных представлен такими симптомами:
- отёчностью ног и покраснением кожи;
- образованием незаживающих язв;
- болезненностью в области груди;
- ощущением нехватки воздуха;
- головными болями;
- онемением конечностей;
- одышкой;
- временными нарушениями остроты зрения, координации и памяти;
- мраморной окраской кожи;
- самопроизвольным прерыванием беременности;
- преждевременной родовой деятельностью.
Кроме этого, велика вероятность отягощённого протекания периода вынашивания ребёнка, что заключается в развитии эклампсии или преэклампсии.
Клинические варианты АФС
Различают первичный и вторичный АФС. В случае отсутствия каких-либо признаков тех или иных заболеваний в течение не менее 5 лет с момента появления первого симптома АФС такой вариант считают первичным. Полагают, что около 50% больных страдают первичной формой АФС. Однако вопрос о нозологической самостоятельности первичного АФС до конца не ясен. Есть данные о том, что первичный АФС может быть вариантом начала СКВ. Наоборот, у некоторых больных с классической СКВ в дебюте в дальнейшем на первый план выходят признаки АФС. Дифференциальный диагноз первичного и вторичного АФС весьма затруднителен. Для первичного АФС не характерно наличие эритемы в виде бабочки, дискоидных высыпаний, фотодерматита, афтозного стоматита, артрита, серозита, синдрома Рейно, антинуклеарного фактора (АНФ) в высоком титре, АТ к нативной ДНК или Sm-антигену. При вторичном АФС чаще отмечаются гемолитическая анемия, тромбоцитопения, лимфопения, нейтропения и низкие уровни С4-компонента комплемента .
Выделяют следующие основные формы АФС:
- АФС у больных с достоверным диагнозом СКВ (вторичный АФС);
- АФС у больных с волчаночноподобными проявлениями;
- первичный АФС;
- «катастрофический» АФС (острая диссеминированная коагулопатия/васкулопатия с острым мультиорганным тромбозом, развивающимся за короткий промежуток времени (от нескольких часов до 7 дней) и приводящим к полиорганной недостаточности);
- другие микроангиопатические синдромы (тромботическая тромбоцитопеническая пурпура, гемолитико-уремический синдром); HELLP-синдром (гемолиз, повышение уровня печеночных ферментов, снижение содержания тромбоцитов, беременность); ДВС-синдром; гипопротромбинемический синдром;
- серонегативный АФС.
«Катастрофический» АФС (КАФС) имеет наиболее тяжелый прогноз. У большинства пациентов с КАФС отмечается микроангиопатия с окклюзией мелких сосудов различных органов, преимущественно почек, легких, головного мозга, сердца и печени. У некоторых больных развивается тромбоз крупных сосудов. Нередко при КАФС тромбоз сочетается с тромбоцитопенией и/или гемолитической анемией .
Развитие КАФС отмечено у больных разного возраста, в том числе и у детей в возрасте до 15 лет. Он нередко возникает при первичном АФС, из ревматических заболеваний – наиболее часто при СКВ и лишь в отдельных случаях при других нозологиях. Следует подчеркнуть, что у 1/2-1/3 больных инициирующими КАФС факторами являются инфекции, что связано с феноменом молекулярной мимикрии между бактериальными антигенами и β2-ГП-1-аутоантигеном. Инициирующими факторами развития КАФС могут быть бактериальные токсины, хирургическое вмешательство, проведение инвазивного инструментального исследования, травмы, отмена антикоагулянтов, назначение ряда медикаментов (тиазидов, каптоприла, эстрогенсодержащих препаратов и др.). При вторичном АФС развитие КАФС может быть обусловлено обострением основного заболевания. Вместе с тем КАФС при СКВ обычно возникает внезапно на фоне умеренной активности заболевания, нередко у пациентов, находящихся на диспансерном мониторинге.
Течение АФС, тяжесть и распространенность тромбозов, их рецидивирование непредсказуемы и в большинстве случаев не коррелируют с изменением титров аФЛ-АТ и активностью СКВ. У одних больных АФС проявляется венозными тромбозами, у других – инсультом, у третьих – акушерской патологией или тромбоцитопенией.
Риск развития тромбоза у больных с АФС очень значителен и достигает 70% после эпизода венозного тромбоза и 90% – после артериального . Он наиболее высок:
а) у лиц молодого возраста с постоянно высоким уровнем аКЛ (β2-ГП-1-зависимой популяции АТ), ВА или АТ к β2-ГП-1;
б) при одномоментном обнаружении аКЛ и ВА;
в) при наличии рецидивирующих тромбозов и/или акушерской патологии в анамнезе;
г) при наличии других факторов риска тромботических нарушений (АГ, гиперлипидемии, курение, прием оральных контрацептивов), при обострении основного заболевания (СКВ), наличии сопутствующих мутаций факторов свертывания крови;
д) при быстрой отмене непрямых антикоагулянтов;
е) при сочетании высоких титров аФЛ-АТ с другими нарушениями свертывания, прежде всего мутацией V фактора свертывания крови, а возможно, и дефицитом других белков (антитромбина-ІІІ, протеинов С и S), гомоцистеинемией.
Как лечат сосудистую патологию Хьюджа
Основная цель комплексной терапии заключается в предотвращении осложнений, вызванных тромбозами. Сложность выбора лечебных мероприятий обусловлена отсутствием достоверной информации о причинах болезни, механизмах ее развития. Схему терапии выстраивают методом проб – если назначенный препарат демонстрирует хороший эффект, им рекомендуется продолжать лечение АФС.
Во время лечения пациенту придется соблюдать ряд жизненно важных правил:
- Уменьшить физическую активность, отказавшись от непосильных нагрузок.
- Не оставаться долгое время в состоянии покоя без движения.
- Придерживаться разработанного медиком режима дня.
- Отказаться от вредных привычек и авиа перелетов.
- Не прекращать прием медикаментов без согласования с врачом.
Терапевтический курс медикаментозного противостояния антифосфолипидному синдрому реализуется по двум направлениям – лечение и профилактика. Сначала купируют признаки острой формы стартовавшего тромбоза, затем переходят к профилактическим мерам, обеспечивающим защиту от эпизодов повторного тромбообразования.
Что назначают при тромбозах
Для выведения пациента из фазы острого тромбоза используют прямые (Гепарин) и непрямые (Варфарин) антикоагулянты. Методика сочетанному принципу позволяет быстро снизить свертываемость крови, что способствует растворению тромбов. Далее подбирают медикаментозную схему лечения, включающую несколько разновидностей препаратов:
- антикоагулянтами (Варфарин и Гепарин), разжижающими кровь, добиваются стойкого снижения показателя ее свертываемости;
- для предотвращения рецидивов и закупорки сосудов сгустками назначают прием ингибиторов тромбоцитов (Клопидогрель, Аспирин);
- глюкокортикостероидами (Преднизолон, Дексаметазон) блокируют воспалительный процесс при системной красной волчанке, сочетающейся с АФС.
Срочные методы помощи включают интенсивную терапию высокими дозами Варфарина и Гепарина. Системный воспалительный процесс купируют глюкокортикостероидами, низкий уровень тромбоцитов восполняют внутривенными вливаниями иммуноглобулина. При отсутствии эффекта от применения интенсивных мер подключают цитотоксические препараты, против высоких титров антител показан плазмофорез для очищения крови.
Методы профилактики
Благодаря своевременной диагностике и методам профилактической терапии удается сдерживать развитие и рецидивирование тромбозов, добиваться благоприятного исхода беременности и неосложненных родов. Для защиты от развития вторичного типа болезни Хьюджа необходимо контролировать основную патологию, обеспечить профилактику инфицирования. Прогноз рискует быть неблагоприятным при сочетании рецидивирующего и артериального тромбозов с тромбоцитопенией и стойким увеличением АТ к уровню кардиолипина.
Подготовка к анализу
Прием препаратов должен быть отменен
Для достоверного результата необходимо придерживаться рекомендаций перед изъятием крови.
- Воздержаться от приёма пищи, алкоголя, курения за 12 часов до анализа.
- В день сдачи анализа не следует употреблять чай или кофе, можно пить обычную воду.
- Все иные исследования (УЗИ, рентгенография) должны проводиться после взятия образца крови.
- На результаты анализа на АФЛ влияют медицинские препараты — гормональные контрацептивы, психотропные, антиаритмические средства, поэтому необходимо исключить их приём за 5 дней до анализа.
- Сдавать кровь для диагностики следует в утреннее время.
Антифосфолипидный синдром при беременности
К сожалению, несвоевременная диагностика и отсутствие лечебных мероприятий, направленных на устранение признаков антифосфолипидного синдрома у беременной женщины может стать причиной тяжелых осложнений, как в период вынашивания плода, так и в момент родоразрешения. В некоторых ситуациях, заключение «антифосфолипидный синдром» устанавливается только лишь после нескольких эпизодов преждевременного прерывания беременности на разных сроках.
Существует статистика, согласно которой даже у абсолютно здоровой беременной женщины в 2% случаев наблюдаются транзиторные эпизоды повышения уровня антифосфолипидных антител, обусловленные иммунными нарушениями и требующими динамического лабораторного контроля без медикаментозной коррекции.
Клинические проявления и степень их проявления зависят не столько от лабораторного титра антифосфолипидных антител, сколько от срока беременности, в течение которой они появились. Так, в первом триместре беременности наличие антител к фосфолипидам может стать провокатором возникновения самопроизвольного аборта. Второй триместр беременности у женщины, страдающей антифосфолипидным синдромом, протекает с признаками внутриутробной задержки развития плода и эпизодами преэклампсии. Третий триместр опасен в отношении развития таких тяжелых осложнений, как внутриутробная гибель плода или преждевременно наступившие роды.
Все вышеперечисленные патологические состояния объясняются тромботическим влиянием антифосфолипидных антител на сосудистую плацентарную систему, обеспечивающую внутриутробное питание плода. Кроме того, антифосфолипидный синдром при беременности запускает каскад гормональных изменений в организме беременной женщины, имеющих большое значение в регуляции процесса внутриутробного развития плода.
Существует четкая зависимость между высоким уровнем антифосфолипидных антител в крови женщины репродуктивного возраста и невозможностью зачатия ребенка, обусловленной нарушением процесса имплантации бластоциста.
В связи с тем, что антифосфолипидный синдром относится к категории заболеваний, провоцирующих тяжелые акушерские патологии, его диагностика должна входить в состав алгоритма обязательного обследования женщин, страдающих бесплодием и привычным невынашиванием плода.
В случае лабораторно подтвержденного антифосфолипидного синдрома, всем пациенткам до наступления беременности рекомендовано применение препаратов глюкокортикоидного ряда в минимальной дозировке (Преднизолон в суточной дозе 5 мг) под постоянным контролем титра антител к фосфолипидам и показателей коагулограммы. В ситуации затяжного течения антифосфолипидного синдрома, беременная женщина вынуждена принимать кортикостероиды весь период беременности, и даже ранний послеродовый период. Длительную гормональную терапию следует проводить «под прикрытием» Иммуноглобулина в дозировке 25 мл курсом трое суток с целью предотвращения возможного рецидива острой вирусной инфекции.
Для того чтобы минимизировать побочные проявления применяемых с лечебной целью при антифосфолипидном синдроме лекарственных средств, рекомендовано проведение тщательного обследования и медикаментозной подготовки пациентки в период планирования беременности.
Минимальные диагностические мероприятия в течение беременности заключаются в проведении оценки степени развития плода по данным ультразвукового исследования с периодичностью не менее 1 раза в месяц, допплерометрии с целью исключения патологии плацентарного кровообращения и в третьем триместре регулярной кардиотокографии.
Лабораторный анализ на антифосфолипидный синдром впервые производится на шестой неделе беременности и непосредственно перед родами. Кроме того, пациенткам с антифосфолипидным синдромом должно систематически проводиться исследование показателей свертывающей системы, включая ранний послеродовый период, в котором имеется высокий риск возникновения тромбоэмболических осложнений.
При имеющихся изменениях коагулограммы, свидетельствующих в пользу активации процесса тромбообразования, всем беременным и родильницам рекомендовано продолжение антикоагулянтной терапии (Гепарин в суточной дозе 10 000 ЕД подкожно), которая является абсолютным противопоказанием для лактации.





Добавить комментарий