О бактериофагах
Содержание:
- Гаметы. Свойства, строение и функции яйцеклетки и сперматозоида
- Значение
- Что такое бактериофаги?
- Фаготерапия по-русски
- Применение
- Инструкция на Бактериофаг стафилококковый (Способ и дозировка)
- Что такое бактериофаги, список препаратов, лечение, преимущества перед антибиотиками
- Взаимодействие бактериофага с бактериальными клетками
- Морфология и строение бактериофагов
- Примечания
Гаметы. Свойства, строение и функции яйцеклетки и сперматозоида
Гаметы
обеспечивают передачу наследственной
информации между поколениями особей.
Это высо-кодифференцированные клетки,
ядра которых содержат всю необходимую
наследственнуюинформацию для развития
нового организма.
По
сравнению ссоматическими клетками
гаметы имеют ряд характерных особенностей.
Первое отличие – наличие в ядре
гаплоидного набора хромосом, что
обеспечивает воспроизведение в зиготе
типичного для организмов данного вида
диплоидного набора.
Второе
отличие – необычное ядерно-цитоплазмати-ческое
соотношение. Уяйцеклеток оно снижено
за счет того, что имеется много цитоплазмы,
где содержится питательный материал
(желток) для будущего зародыша. В
сперматозоидах, наоборот,
ядерно-цито-плазматическое соотношение
высокое, так как мал объем цитоплазмы.
Третье
отличие – низкий уровень обмена веществ
в гаметах. Их состояние похоже на анабиоз.
Мужские половые клетки вообще не вступают
в митоз, а женские гаметы получают эту
способность только после оплодотворения
или воздействия фактора, индуцирующего
партеногенез.
Яйцеклетка
– крупная неподвижная клетка, обладающая
запасом питательных веществ. Размеры
женской яйцеклетки составляют 150–170
мкм. Функции питательных веществ
различны. Их выполняют:
1) компоненты,
нужные для процессов биосинтеза белка;
2) специфические
регуляторные вещества;
3) желток
обеспечивающий питание зародыша в
эмбриональном периоде.
Яйцеклетка
имеет оболочки, которые препятствуют
проникновению в яйцеклетку более одного
сперматозоида.
Яйцеклетка
обычно имеет шарообразную или слегка
вытянутую форму, снаружи окружена
блестящей оболочкой, которая покрыта
лучистым венцом, или фолликулярной
оболочкой. Она играет защитную роль,
питает яйцеклетку.
Яйцеклетка
лишена аппарата активного движения.
Для яйцеклетки характерна плазматическая
сегрегация.
Сперматозоид
– это мужская половая клетка (гамета).
Он обладает способностью к движению.
Размеры сперматозоида микроскопические:
длина этой клетки у человека составляет
50–70 мкм.
Строение
сперматозоида
Сперматозоид
имеет головку, шейку, промежуточный
отдел и хвост в виде жгутика. Почти вся
головка заполнена ядром, которое несет
наследственный материал в виде хроматина.
На переднем конце головки (на ее вершине)
располагается акросома, которая
представляет собой видоизмененный
комплекс Гольджи. Здесь происходит
образование гиалуронидазы – фермента,
который способен расщеплять
мукополисаха-риды оболочек яйцеклетки.
В шейке сперматозоида расположена
митохондрия, которая имеет спиральное
строение. Она необходима для выработки
энергии, которая тратится на активные
движения сперматозоида по направлению
к яйцеклетке. Оболочка сперматозоида
имеет специфические рецепторы, которые
узнают химические вещества, выделяемые
яйцеклеткой. Поэтому сперматозоиды
человека способны к направленному
движению по направлению к яйцеклетке
(это называется положительным
хемотаксисом).
Значение
Строение вирусов на примере бактериофага может нам о многом сказать, особенно для взаимодействия с другой информацией, которой располагает о них человек. Например, они являются, предположительно, самой древней формой вирусных частиц. Количественный анализ указывает нам на то, что их популяция имеет более 1030 частиц.
В природе их можно обнаружить там же, где обитают и бактерии, к которым они могут проявлять чувствительность. Так как рассматриваемые организмы определяются по месту обитания, предпочтениями бактерий, которых они поражают, то, следовательно, лизирующие почвенных бактерий (фаги) будут жить в почве. Чем больше в субстрате содержится микроорганизмов, тем больше там и необходимых фагов.
В действительности каждый бактериофаг воплощает в себе одну из основных элементных единиц генетической подвижности. Используя трансдукцию, они обуславливают возникновение новых генов в наследственном материале бактерии. За секунду может произойти инфицирование около 1024 бактериальных клеток. Такая форма ответа на вопрос о том, какие вирусы называются бактериофагами, открыто показывает нам способы распределения наследственной информации, происходящие между бактериальными организмами из общей среды обитания.
Что такое бактериофаги?
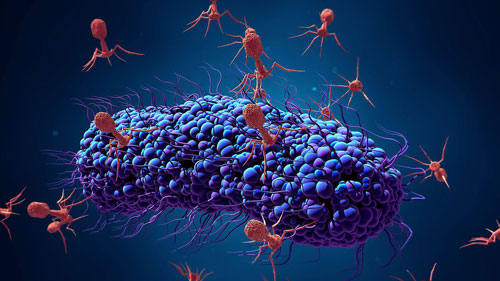
Бактериофаги, также известные как фаги, представляют собой вирусы, которые инфицируют и размножаются только в бактериальных клетках. Они повсеместно распространены в окружающей среде и признаны самым распространенным биологическим агентом на Земле. Они чрезвычайно разнообразны по размеру, морфологии и геномной организации. Однако все они состоят из генома нуклеиновой кислоты, заключенного в оболочку из кодируемых фагами капсидных белков, которые защищают генетический материал и опосредуют его доставку в следующую клетку-хозяин. Электронная микроскопия позволила детально визуализировать сотни типов фагов, некоторые из которых имеют «головы», «ноги» и «хвосты». Несмотря на это, бактериофаги неподвижны и зависят от броуновского движения для достижения своих целей.
Как и все вирусы, бактериофаги очень видоспецифичны по отношению к своим хозяевам и обычно заражают только один вид бактерий или даже определенные штаммы внутри вида. Как только бактериофаг прикрепляется к восприимчивому хозяину, он реализует одну из двух стратегий репликации: литическую или лизогенную.
Во время цикла литической репликации фаг прикрепляется к восприимчивой бактерии-хозяину, вводит свой геном в цитоплазму клетки-хозяина и использует рибосомы хозяина для производства своих белков. Ресурсы клетки-хозяина быстро превращаются в вирусные геномы и капсидные белки, которые собираются в несколько копий исходного фага. Когда клетка-хозяин умирает, она активно или пассивно лизируется, высвобождая новый бактериофаг для заражения другой клетки-хозяина.
В цикле лизогенной репликации фаг также прикрепляется к восприимчивой бактерии-хозяину и вводит свой геном в цитоплазму клетки-хозяина. Однако геном фага вместо этого интегрируется в хромосому бактериальной клетки или поддерживается как эписомальный элемент, где в обоих случаях он реплицируется и передается дочерним бактериальным клеткам, не убивая их. Интегрированные фаговые геномы называются профагами, а содержащие их бактерии — лизогенами. Профаги могут вернуться в цикл литической репликации и убить своего хозяина, чаще всего в ответ на изменение условий окружающей среды.
Фаготерапия по-русски
Эксперты отмечают, что производство бактериофагов – весьма перспективное направление в фармацевтической промышленности. Кстати, наша страна в производстве бактериофагов исторически занимает ведущие позиции. Уже в годы Великой Отечественной войны применялась фаготерапия
Особое внимание уделялось разработке бактериофагов против кишечных инфекций – холеры, брюшного тифа, дизентерии и сальмонеллеза. Всего в военное время для фронта было изготовлено более 200 тыс
литров бактериофагов.
Сегодня в нашей стране развитие производства лекарственных препаратов на основе бактериофагов входит в Стратегию предупреждения распространения антимикробной резистентности в Российской Федерации до 2030 года, принятую Правительством РФ. Единственный в стране производитель препаратов бактериофагов – компания «Микроген» холдинга «Нацимбио» Госкорпорации Ростех. В период с 2017 по 2019 год продажи бактериофагов «Микрогена» выросли более чем на 25% в денежном выражении.
Компанией разработаны и выпускаются 19 наименований лекарств на основе бактериофагов против множества известных возбудителей инфекционных заболеваний: дизентерии, брюшного тифа, сальмонеллеза, гнойно-септических и других. Кроме того, разработаны комбинированные препараты, например «Секстафаг» (Пиобактериофаг поливалентный). Он обладает способностью справиться с бактериями стафилококков, стрептококков (в том числе энтерококков), протея, клебсиелл пневмонии, синегнойной и кишечной палочек. Данный препарат отличается высокой степенью очистки от бактериальных метаболитов, что позволяет успешно использовать его для лечения новорожденных и детей раннего возраста, а также применять для беременных.
В рамках Стратегии по борьбе с антимикробной резистентностью ученые НПО «Микроген» проводят множество исследований. В настоящий момент предприятие приступило к созданию первого в России Биологического ресурсного центра для углубленного изучения бактериофагов.
«Задача Биологического ресурсного центра – объединить микробные производственные коллекции, собранные на территории России. На данный момент это более 10 тыс. штаммов. В коллекцию также входят бактериофаги для терапевтических целей. Это уникальный материал, представляющий собой государственную ценность, на его основе удастся создать новые виды лекарств», – прокомментировал исполнительный директор Госкорпорации Ростех Олег Евтушенко.
Но, пожалуй, самой амбициозной целью нового центра является создание основы для перехода к персонализированной фаготерапии в ближайшие 5-7 лет. Персонально подобранный «коктейль» из бактериофагов может спасти жизнь пациентам, которым уже не помогают антибиотики.
Успехи российских и зарубежных ученых вселяют надежду на то, что проблема антимикробной резистентности в скором времени может быть преодолена. Тем временем каждый из нас в этой борьбе с «супербактериями» может внести свой маленький вклад – соблюдать правила, которые помогут уберечься от вирусов и бактерий, остановить появление новых опасных инфекций. Все просто: не забывать о гигиене, вести здоровый образ жизни, вовремя обращаться к врачам и ограничить использование антибиотиков.
Применение
В медицине
Одной из областей использования бактериофагов является антибактериальная терапия, альтернативная приёму антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллёзный, дизентерийный поливалентный, пиобактериофаг, коли, протейный и колипротейный и другие. В России зарегистрировано и применяется 13 медицинских препаратов на основе фагов. В настоящее время их применяют для лечения бактериальных инфекций, которые не чувствительны к традиционному лечению антибиотиками, особенно в республике Грузия. Обычно, применение бактериофагов сопровождается большим, чем антибиотики, успехом там, где присутствуют биологические мембраны, покрытые полисахаридами, через которые антибиотики обычно не проникают. В настоящее время терапевтическое применение бактериофагов не получило одобрения на Западе, хотя и применяются фаги для уничтожения бактерий, вызывающих пищевые отравления, таких, как листерии. В многолетнем опыте в объёме крупного города и сельской местности доказана необычайно высокая лечебная и профилактическая эффективность дизентерийного бактериофага (П. М. Лернер, 2010)[источник не указан 1950 дней]. В России терапевтические фаговые препараты делают давно, фагами лечили ещё до антибиотиков. В последние годы фаги широко использовали после наводнений в Крымске и Хабаровске, чтобы предотвратить дизентерию.
В биологии
Бактериофаги применяются в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция).
Фаговые векторы обычно создают на базе умеренного бактериофага λ, содержащего двухцепочечную линейную молекулу ДНК. Левое и правое плечи фага имеют все гены, необходимые для литического цикла (репликации, размножения). Средняя часть генома бактериофага λ (содержит гены, контролирующие лизогению, то есть его интеграцию в ДНК бактериальной клетки) не существенна для его размножения и составляет примерно 25 тысяч пар нуклеотидов. Данная часть может быть заменена на чужеродный фрагмент ДНК. Такие модифицированные фаги проходят литический цикл, но лизогения не происходит. Векторы на основе бактериофага λ используют для клонирования фрагментов ДНК эукариот (то есть более крупных генов) размером до 23 тысяч пар нуклеотидов (т. п. н.). Причём, фаги без вставок — менее 38 т. п. н. или, напротив, со слишком большими вставками — более 52 т. п. н. не развиваются и не поражают бактерии.
Бактериофаги M13, фаг Т4, T7 и фаг λ используют для изучения белок-белковых, белок-пептидных и ДНК-белковых взаимодействий методом фагового дисплея.
Поскольку размножение бактериофага возможно только в живых клетках, бактериофаги могут быть использованы для определения жизнеспособности бактерий. Данное направление имеет большие перспективы, поскольку, одним из основных вопросов при разных биотехнологических процессах является определение жизнеспособности используемых культур. С помощью метода электрооптического анализа клеточных суспензий была показана возможность изучения этапов взаимодействия фаг-микробная клетка.
Инструкция на Бактериофаг стафилококковый (Способ и дозировка)
Препарат вводится в очаг инфекции. Кратность введений и их размер устанавливают с помощью определения клинической формы заболевания, характера инфекционного очага и стандартных рекомендаций. Средняя длительность лечения составляет 5-15 дней. При случаях рецидивов возможно проведение дополнительных курсов лечения. Инструкция по применению бактериофага стафилококкового для детей и для взрослых несколько отличается. Рекомендации по применению препарата для детей приведены в конце раздела.
Жидкий фаг разрешено применять местно в виде примочек, орошения или тампонирования в объеме до 200 мл учитывая размеры участка поражения. Также для местного применения служит мазь.
Терапию гнойно-воспалительных ограниченных поражений целесообразно проводить как местным, так и пероральным способом в течении 1-4 недель.
При гнойно-воспалительных поражениях горла, уха или носа препарат применяют для полоскания, закапывания, промывания и введения смоченных турунд по 2-10 мл до трех раз в день.
При карбункулах и фурункулах жидкий бактериофаг инъецируется непосредственно в очаг или вокруг него, ежедневно по 0,5-2 мл. Всего за курс лечения производят до 5 инъекций.
Лечение хронических остеомиелитов осуществляют вливанием препарата в рану сразу после хирургической обработки.
При абсцессах бактериофаг инъекционно вводится в полость, опустошенного от гноя очага. При вскрытии абсцесса в рану вводят тампон, смоченный препаратом.
Лечение глубокого пиодермита осуществляют произведением внутрикожных инъекций средства в одно место по 0,1-0,5 мл или в несколько мест в суммарной дозе до 2 мл. Введения производят каждые 24 часа, всего 10 инъекций.
Для введения в брюшную, плевральную, суставную полости используют капиллярный дренаж, вводят до 100 мл бактериофага через день. Всего 3-4 таких введения.
При циститах средство вводят в мочевой пузырь с помощью катетера.
При гнойных бурситах, плевритах или артритах препарат вводят в полость, предварительно опустошенную от гноя по 20 мл через день. Курс лечения составляет 3-4 введения.
Также Стафилококковый бактериофаг используют перорально в виде таблеток при лечении урогенитальных инфекций (цистита, пиелонефрита, пиелита, сальпингоофорита, эндометрита), кишечных инфекций и иных заболеваний, вызванных стафилококком.
Как применять Бактериофаг стафилококковый при кишечных стафилококковых поражениях и дисбактериозе кишечника: препарат используют перорально внутрь натощак трижды в сутки за 2 часа до еды; ректально в виде свечей или клизм препарат назначают один раз вдень. Лечение проводят 7-10 дней.
Новорожденным детям в первые 2 приема препарат разводят равным количеством воды. Также его можно перемешивать с грудным молоком.
При сепсисе или энтероколите у новорожденных средство применяют постановкой высоких клизм до трех раз в сутки. Разрешено сочетание ректального и орального применения.
При терапии пиодермий, омфалитов, гнойных ран у новорожденных препарат используют в виде аппликаций дважды в день и в виде таблеток – по 1 штуке до четырех раз в день. Мазь используют локально с повязками по 5-20 грамм до двух раз в день.
При профилактике энтероколита и сепсиса у новорожденных при опасности развития госпитальной инфекции или внутриутробном инфицировании препарат используют в виде клизм дважды в день на протяжении недели.
В аэрозольной форме Бактериофаг стафилококковый используют с целью орошения пораженных слизистых оболочек и кожи при гнойно-воспалительных поражениях, ожогах, септических ранах и ангине.
Наиболее обосновано применение данного средство в случаях инфицирования антибиотикоустойчивыми штаммами.
Что такое бактериофаги, список препаратов, лечение, преимущества перед антибиотиками
Обновление: Октябрь 2018
Бактериофаги представляют собой вирусы, избирательно поражающие бактериальные клетки. Их жизнедеятельность и репродукция возможна только внутри бактериальных клеток. Размножаясь внутри клетки, они вызывают разрушение и гибель самой бактерии.
Современная медицина рассматривает их как эффективное, безопасное и совершенное средство в борьбе с опасными, трудно поддающимися терапии бактериальными инфекциями. Но лечение бактериофагами у многих людей вызывает недоверие и страх.
Особенности строения и паразитирования бактериофагов
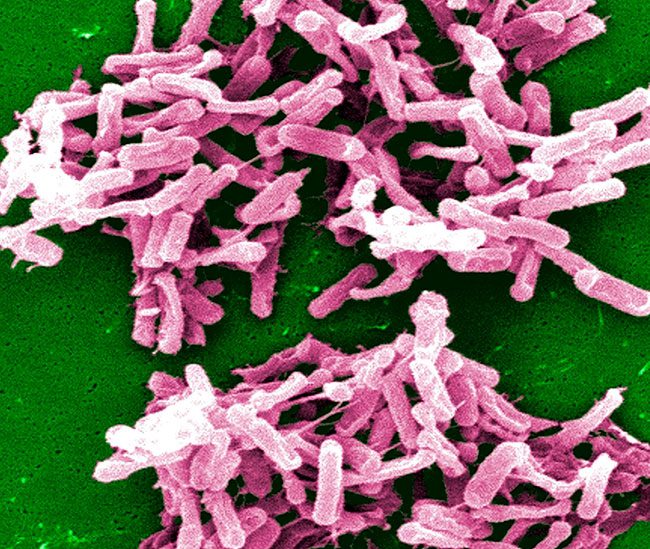
Бактериофаги представляют большую и разнообразную группу вирусов. Их размеры в сто раз меньше размеров бактериальных клеток. При многократном увеличении структура фагов поражает своим разнообразием, некоторые из них похожи на кристаллические комплексы, причудливо извитые между собой.
Являясь внутриклеточными вирусными паразитами, они избирательно уничтожают определенные бактериальные клетки. Они лишены клеточного строения и состоят только из генетического материала, покрытого наружной белковой оболочкой. Это вынуждает их искать подходящие клеточные комплексы, чтобы активно размножаться внутри них.
Среда обитания бактериофагов
Бактериофаги присутствуют везде, где живут бактерии, поэтому среда их обитания разнообразна. Это может быть организм человека, воздушная и водная среда, почва, пищевые продукты, одежда и т.д.
Механизм действия
Бактериофаг внедряется в бактериальную клетку лишь с одной целью – использовать ее клеточные структуры для собственного размножения. Для этого умный вирус впрыскивает в тело бактерии собственную генетическую информацию.
Бактерия же начинает по установленной фагом программе синтезировать нехарактерные для нее частицы, из которых впоследствии осуществляется сборка новых бактериофагов.
От бактериальной клетки остаются одни обломки, через которые выходит 100-200 синтезированных фагов, способных к дальнейшему поражению соседних бактериальных клеток.
В естественной среде бактериофаги играют важнейшую роль природных регуляторов количества патогенных микробов.
Сферы применения бактериофагов
Помимо медицинской отрасли, они нашли свое применение и в других важных направлениях.
- В сельском хозяйстве — успешно применяются для предупреждения и лечения растений и животных от бактериальных инфекций.
- В генной инженерии — эти маленькие вирусные структуры используются для естественного обмена генами между различными бактериями, что позволяет изменять первоначальную структуру бактериальной ДНК в нужном направлении.
Преимущества бактериофагов перед антибиотиками:
- Не угнетают иммунитет человека;
- Сочетаются абсолютно со всеми лекарственными препаратами, даже с антибиотиками, усиливая их действие;
- Не вызывают привыкания;
- Не приводят к выработке устойчивости бактериальных культур к фагам;
- Помогают в лечении вялотекущих бактериальных инфекций, малочувствительных к антибиотикам;
- Действуют избирательно, не уничтожая полезную бактериальную флору;
- Не имеют противопоказаний к лечению.
Их используют в лечении различных инфекций бактериальной природы. Поскольку размножение фагов происходит исключительно в бактериях, никакого вреда здоровью они не приносят. Бактериофаги действуют избирательно, поражая бактерии определенной группы. Наиболее широко используется стафилококковый бактериофаг, эффективный в лечении хронических стафилококковых инфекций и бактерионосительства.
Список препаратов бактериофагов
- Сальмонеллезный для приема внутрь 100мл — 650-800 руб
- Коли бактериофаг 20мл. 4 шт. 400-800 руб, колипротейный для приема внутрь 100мл — 650-800 руб.
- Стрептококковый для приема внутрь, местного и наружного применения 20 мл. 4 шт. — 750-800 руб.
- Клебсиелл поливалентный для приема внутрь 20 мл.
4 шт — 750-800 руб.
- Клебсифаг (клебселл пневмонии) 20мл. 4 шт. 500 руб.
- Дизентерийный поливалентный 80мг. 500 табл. 3400 руб, 20мл. 4 шт -400 руб.
- Протейный бактериофаг 20мл. 4 шт. 500-600 руб.
- Синегнойный бактериофаг/псевдомонас 100мл. и 20мл. 4шт. — 650-700 руб.
Комплексные бактериофаги:
- ИНТЕСТИ комплексный бактериофаг 20мл. 4 шт. и 100мл. для приема внутрь — 800 руб.
- Пиобактериофаг 100 мл. — 800 руб.
- Пиобактериофаг поливалентный очищенный 20мл. 4 шт. — 800 руб.
- Секстафаг Пиобактериофаг поливалентный 20мл. 4 шт. — 750 руб.
Сабук Татьяна Леонидовна врач-гигиенист, эпидемиолог
Взаимодействие бактериофага с бактериальными клетками
Адсорбция бактериофагов на поверхности бактериальной клетки
По характеру взаимодействия бактериофага с бактериальной клеткой различают вирулентные и умеренные фаги.
Вирулентные фаги могут только увеличиваться в количестве посредством литического цикла. Процесс взаимодействия вирулентного бактериофага с клеткой складывается из нескольких стадий: адсорбции бактериофага на клетке, проникновения в клетку, биосинтеза компонентов фага и их сборки, выхода бактериофагов из клетки.
Первоначально бактериофаги прикрепляются к фагоспецифическим рецепторам на поверхности бактериальной клетки. Хвост фага с помощью ферментов, находящихся на его конце (в основном лизоцима), локально растворяет оболочку клетки, сокращается и содержащаяся в головке ДНК инъецируется в клетку, при этом белковая оболочка бактериофага остаётся снаружи. Инъецированная ДНК вызывает полную перестройку метаболизма клетки: прекращается синтез бактериальной ДНК, РНК и белков. ДНК бактериофага начинает транскрибироваться с помощью собственного фермента транскриптазы, который после попадания в бактериальную клетку активируется. Синтезируются сначала ранние, а затем поздние иРНК, которые поступают на рибосомы клетки-хозяина, где синтезируются ранние (ДНК-полимеразы, нуклеазы) и поздние (белки капсида и хвостового отростка, ферменты лизоцим, АТФаза и транскриптаза) белки бактериофага. Репликация ДНК бактериофага происходит по полуконсервативному механизму и осуществляется с участием собственных ДНК-полимераз. После синтеза поздних белков и завершения репликации ДНК наступает заключительный процесс — созревание фаговых частиц или соединение фаговой ДНК с белком оболочки и образование зрелых инфекционных фаговых частиц.
Продолжительность этого процесса может составлять от нескольких минут до нескольких часов. Затем происходит лизис клетки, и освобождаются новые зрелые бактериофаги.
Иногда фаг инициирует лизирующий цикл, что приводит к лизису клетки и освобождению новых фагов. В качестве альтернативы фаг может инициировать лизогенный цикл, при котором он вместо репликации обратимо взаимодействует с генетической системой клетки-хозяина, интегрируясь в хромосому или сохраняясь в виде плазмиды. Таким образом, вирусный геном реплицируется синхронно с ДНК хозяина и делением клетки, а подобное состояние фага называется профагом. Бактерия, содержащая профаг, становится лизогенной до тех пор, пока при определённых условиях или спонтанно профаг не будет стимулирован на осуществление лизирующего цикла репликации. Переход от лизогении к лизису называется лизогенной индукцией или индукцией профага. На индукцию фага оказывает сильное воздействие состояние клетки хозяина предшествующее индукции, также как наличие питательных веществ и другие условия, имеющие место в момент индукции. Скудные условия для роста способствуют лизогенному пути, тогда как хорошие условия способствуют лизирующей реакции.
Очень важным свойством бактериофагов является их специфичность: бактериофаги лизируют культуры определённого вида, более того, существуют так называемые типовые бактериофаги, лизирующие варианты внутри вида, хотя встречаются поливалентные бактериофаги, которые паразитируют в бактериях разных видов.
Морфология и строение бактериофагов
Вирусы, поражающие бактерий, актиномицеты
и грибы, называются бактериофагами или
просто фагами. Они имеют некоторые
особенности необходимо рассмотреть
несколько подробнее.
Строение фага более сложно, чем строение
вирусов животных и растений. Довольна,
своеобразна морфология фага. У него
различают головку, имеющую овальную
форму
иногда шестигранную, призматическую,
иногда круглую. От головки отходит более
или менее длинный полый отросток. Фаг
сравнивают с барабанной, палочкой,
булавкой, головастиком. По своим размерам
фаги относятся к средним по величине
вирусам. Диаметр головки их составляет
60-90 мкм, длина отростка — 250 мкм, толщина
— 10-25 мкм. Величина фагов довольно
изменчива. Даже разные варианты одного
и того же вида фага могут сильно
различаться по своим размерам. Молекулярный
вес фага 200 млн.
Частица фага является нуклеопротеидом
и состоит из белка (50-60%) и ДНК (45-50%),которые
фаги содержат небольшое количество
липидов (1,5-2%). Белок образует оболочку
фага, а ДНК находится во внутреннем
пространстве головки фага. Белковая
оболочка состоит из большого числа
белковых частиц называемых субъединицами.
Примечания
- ↑
- Ackermann H.-W. // Res. Microbiol., 2003. — V. 154. — P. 245—251
- Hendrix R.W. // Theor. Popul. Biol., 2002. — V. 61. — P. 471—480
- Шестаков С. В. Как происходит и чем лимитируется горизонтальный перенос генов у бактерий. Экологическая генетика 2007. — Т. 5. — № 2. — C. 12-24.
- ↑
- ↑ Guttman B., Raya R., Kutter E. Basic Phage Biology, in Bacteriophages: Biology and Applications, (Kutter E. and Sulakvelidze A., ed.), CRP Press, 2005 FL. — P. 29-66.
- Ковалёва Е. Н. Создание биопрепарата на основе выделенных и изученных бактериофагов Enterococcus faecalis: Дис. … канд. биол. наук. — Саратов, 2009. — 151 с.
- Ackermann H.-W. // Res. Microbiol., 2003. — V. 154. — P. 245—251.
- ↑ Ожерельева Н. Г. Краткая Медицинская Энциклопедия, М.: изд-во «Советская Энциклопедия», 1989. — издание второе.
- Бактериофаги // : / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Molecular Medical Microbiology / Yi-Wei Tang, Max Sussman, Dongyou Liu, Ian Poxton, Joseph Schwartzman. — 2 ed. — Academic Press, 2014. — Vol. 1. — P. 579. — 2216 p. — ISBN 9780123977632.
- Virus Taxonomy. Classification and Nomenclature of Viruses. Seventh Report of the International Committee on Taxonomy of Viruses / Edited by M.H.V. van Regenmontel et al. — San Diego: Academic Press, 2000. — P. 43-53, 64-129.
- Raya R.R., Hébert E.M. Isolation of phage via induction of lysogens. Bacteriophages: Methods and Protocols, Volume 1: Isolation, Characterization, and Interaction (Martha R.J. Clokie, Andrew M. Kropinski (eds.), 2009. — V. 501. — P. 23-32.
- ↑ Микробиология: учеб. пособие / В. В. Лысак. — Минск: БГУ, 2007. — 430 с.
- Адамс М. Бактериофаги / М. Адамс. — М.: Медгиз, 1961. — 521 с.
- Гольдфарб Д. М., Бактериофагия / Д. М. Гольдфарб. — М.: Медгиз, 1961. — 299 с.
- BBC Horizon: Phage — The Virus that Cures 1997-10-09
- Щелкунов С. Н. Генетическая инженерия / С. Н. Щелкунов. — Новосибирск: Сиб. унив. изд-во, 2004. — 496 с.
- Guliy O.I., Bunin V.D., O’Neil D., Ivnitski D., Ignatov O.V. A new electro-optical approach to rapid assay of cell viability // Biosensors and Bioelectronics. 2007. V. 23. P. 583—587.




Добавить комментарий